Что нужно знать, как определять продукты и как решать задания формата №20
Электролиз — одна из обязательных тем ЕГЭ. Она встречается:
Чтобы уверенно решать такие задания, нужно понимать, кто разряжается на аноде и катоде, и помнить порядок восстановления катионов и окисления анионов в воде.
Электролиз — одна из обязательных тем ЕГЭ. Она встречается:
- в задании №20 части 1 (часто — электролиз солей в растворе);
- в органической и неорганической части (электролиз расплавов, получение металлов и галогенов);
- в задачах с разбором механизмов окисления и восстановления.
Чтобы уверенно решать такие задания, нужно понимать, кто разряжается на аноде и катоде, и помнить порядок восстановления катионов и окисления анионов в воде.
📘 Какие типы электролиза встречаются в ЕГЭ?
1) Электролиз водных растворов (самый частый)
Нужно определить, кто восстановится на катоде (–) и кто окислится на аноде (+)
Важно помнить: в растворе есть ионы соли + ионы воды.
2) Электролиз расплавов
Здесь воды нет → разряжаются только катион и анион соли.
Этот тип встречается в заданиях на получение металлов (Na, Mg, Al).
3) Электролиз в задачах на способы получения веществ
Например, как получить алюминий или фтор — в демоверсии-2026 прямо указано:
- Al — электролиз расплава Al₂O₃ в криолите,
- F₂ — электролиз расплава KF,
- К — электролиз расплава KF.
📚 Главные правила для электролиза в растворе (для ЕГЭ)
✔ На катоде (–) — восстановление
Восстанавливаются:
- металлы активнее водорода → Н₂ выделяется
- металлы менее активные, чем водород → выделяется металл
Правило:
K, Na, Ca, Mg, Al, Zn, Fe → водород
Cu²⁺, Ag⁺, Au³⁺ → металл
✔ На аноде (+) — окисление
- Если анион — галогенид (Cl⁻, Br⁻, I⁻) → выделяется галоген
- Если анион — сульфат, нитрат → окисляется вода → кислород
📘 Применим эти правила к заданию №20 демоверсии ЕГЭ-2026
В демоверсии дано задание:
Установите соответствие между солью и продуктами электролиза её водного раствора на инертных электродах
Варианты соли:
А) нитрат ртути(II)
Б) нитрат рубидия
В) хлорид алюминия
Варианты продуктов:
- водород, галоген
- водород, кислород
- металл, кислород
- металл, галоген
✔ Разбор по каждому веществу
🔹 А) Нитрат ртути(II), Hg(NO₃)₂
Катион: Hg²⁺ (благородный металл)
→ восстанавливается сам металл: Hg
Анион: NO₃⁻
→ вода окисляется до O₂
✔ Продукты: металл + кислород
Ответ: 3
🔹 Б) Нитрат рубидия, RbNO₃
Катион: Rb⁺ — очень активный металл
→ восстанавливается вода → H₂
Анион: NO₃⁻
→ окисляется вода → O₂
✔ Продукты: водород + кислород
Ответ: 2
🔹 В) Хлорид алюминия, AlCl₃
Катион: Al³⁺ (активный металл)
→ восстанавливается вода → H₂
Анион: Cl⁻
→ окисляется до Cl₂
✔ Продукты: водород + галоген
Ответ: 1
🎯 Итог по заданию №20 (демоверсия-2026)
✔ Итоговый ответ:
3 2 1
📘 Электролиз органических веществ (в ЕГЭ встречается редко)
В заданиях ЕГЭ могут мелькать реакции электролиза, ведущие к:
- образованию радикалов,
- отщеплению CO₂ у солей карбоновых кислот (электролиз Кольбе),
- образованию алканов/алкенов.
Главный пример:
электролиз ацетата натрия:
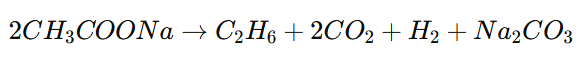
Используется в заданиях на органику (обычно 24, 29, 32).
📌 Мини-шпаргалка easyknow: электролиз в 10 строках
Катод:
- Активные металлы (K–Fe) → H₂
- Малоактивные (Cu, Ag, Au) → металл
Анод:
- Галогениды → галоген (Cl₂, Br₂, I₂)
- NO₃⁻, SO₄²⁻ → O₂
Расплавы:
- Разряжаются ионы соли → всегда металл + неметалл
Органика:
- Соли карбоновых кислот → радикалы → углеводороды
🎯 Итог
Задания на электролиз в ЕГЭ — это чистая логика + три правила.
Если запомнить порядок разрядов катионов и анионов, задачи любой сложности решаются за 20–30 секунд.
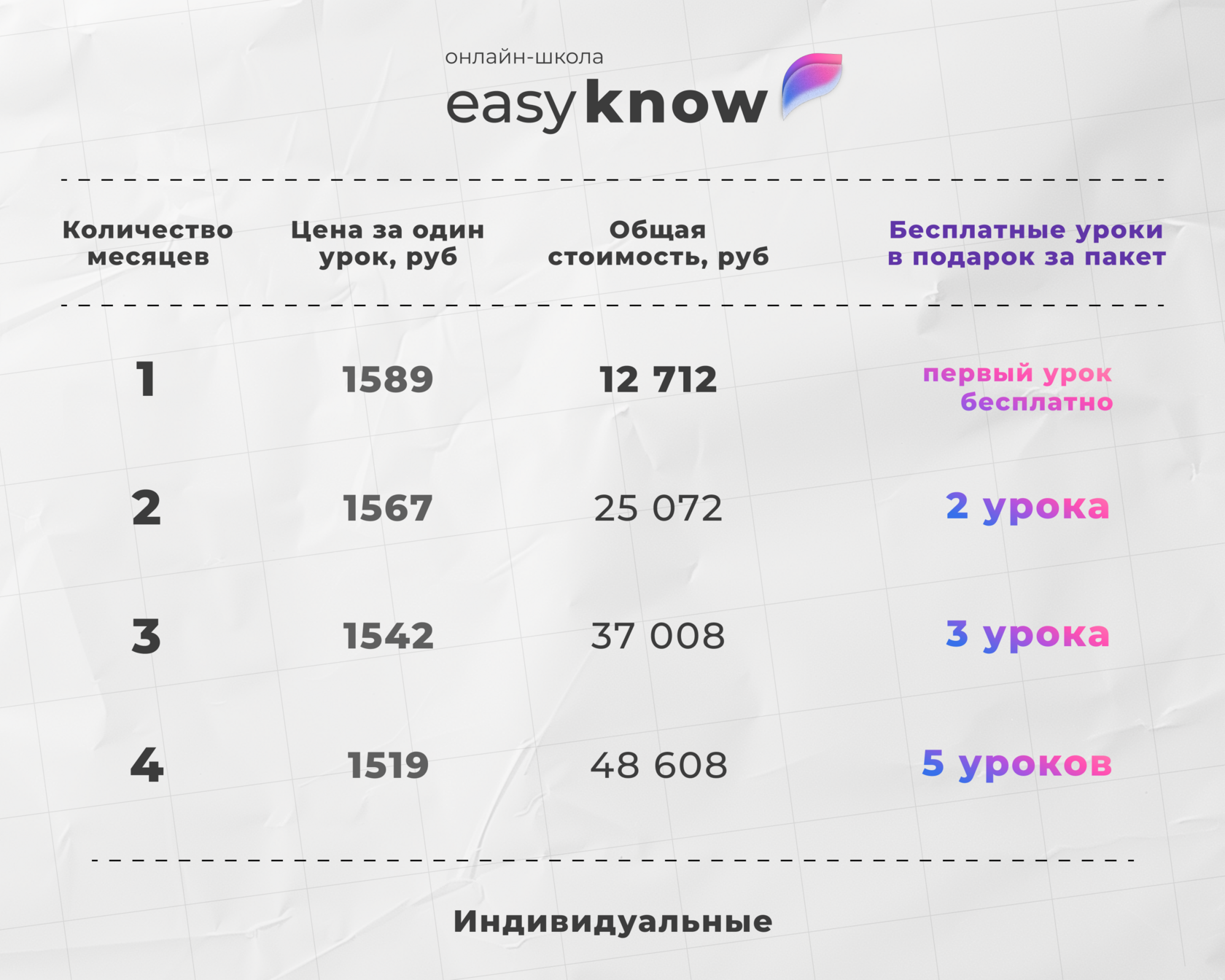
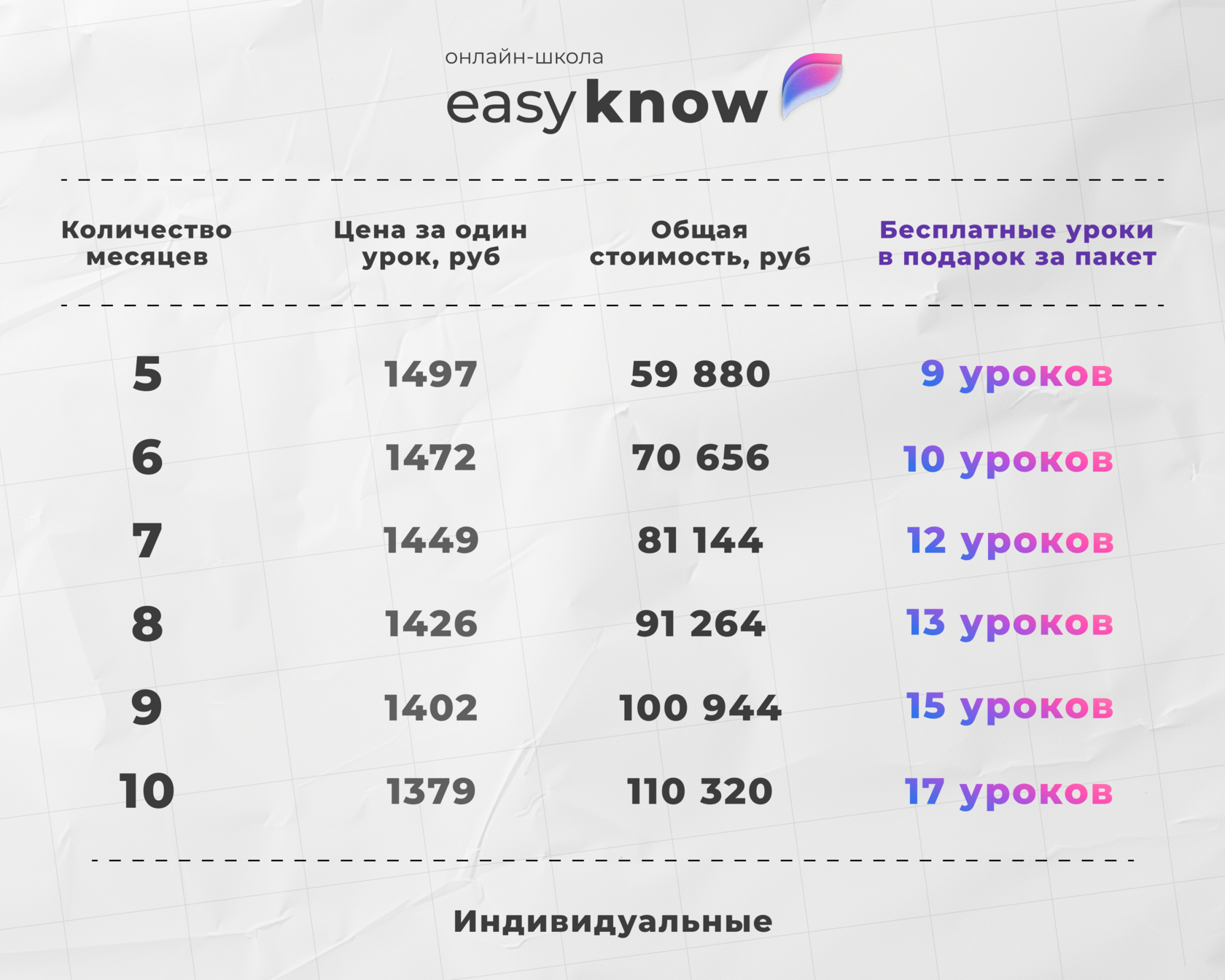
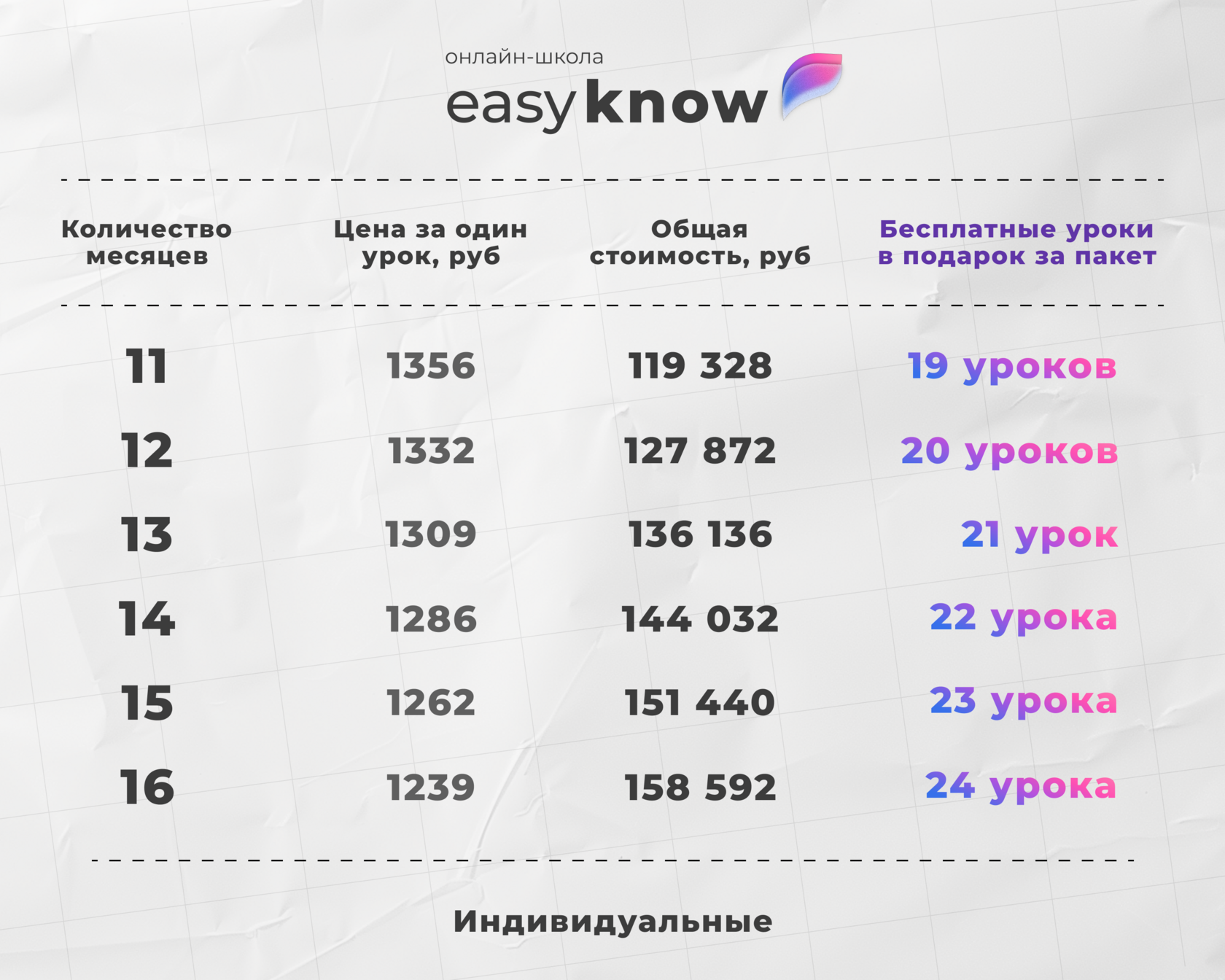
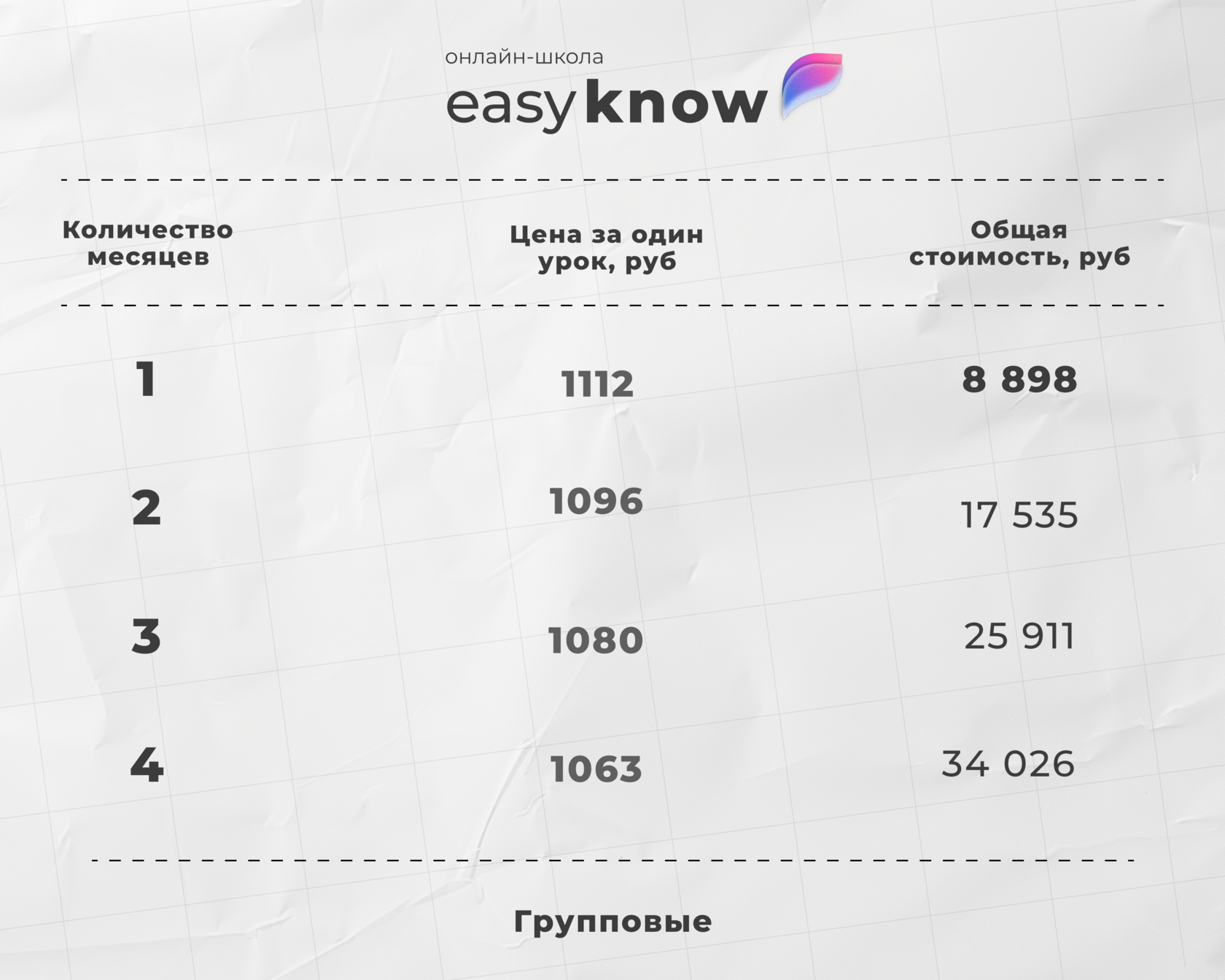
Эта статья — лишь фрагмент знаний. На платформе Easyknow вся подготовка становится системой: от большой коллекции материалов по разным предметам до домашних заданий с проверкой. Всё в одном месте, по вашему личному плану.
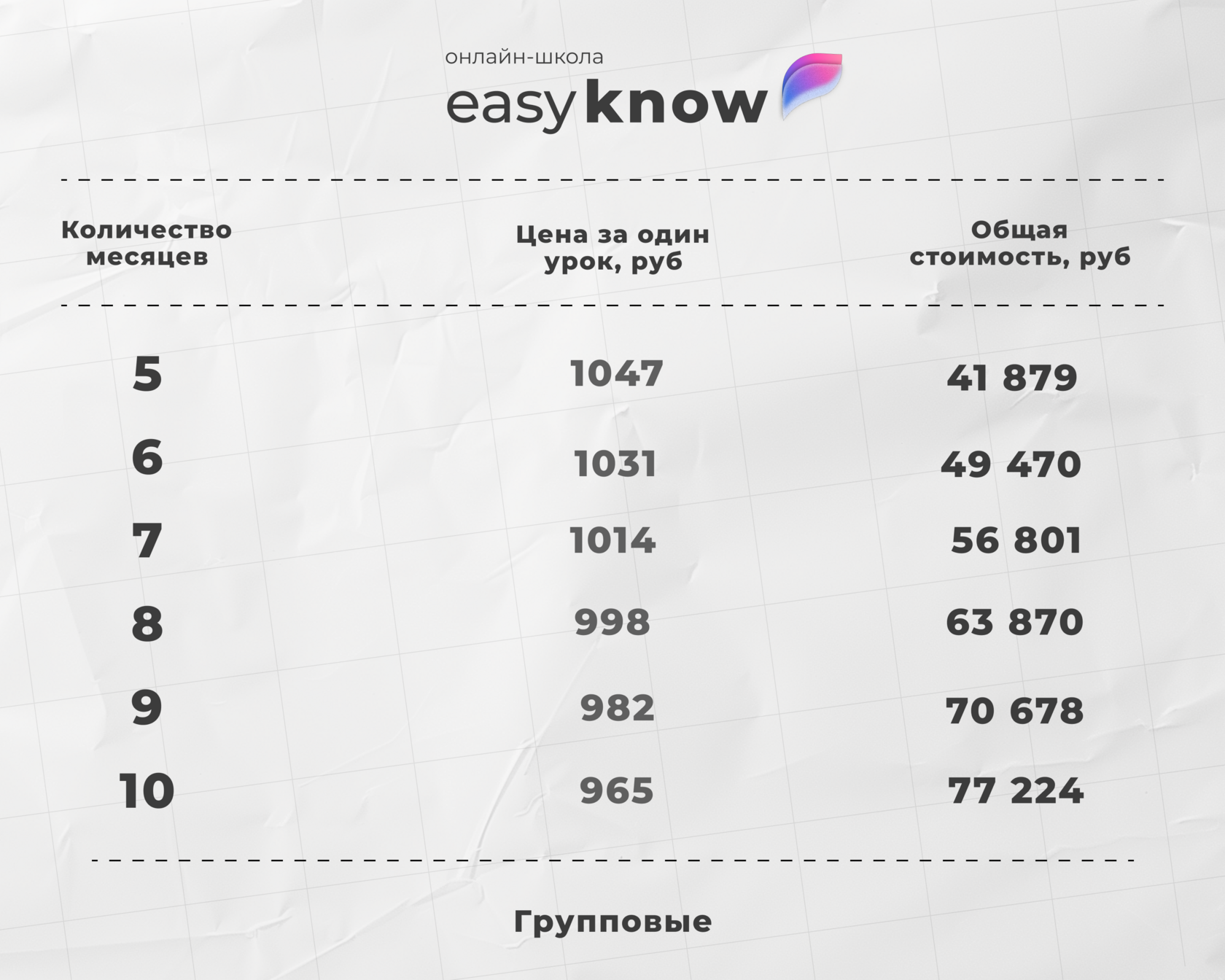
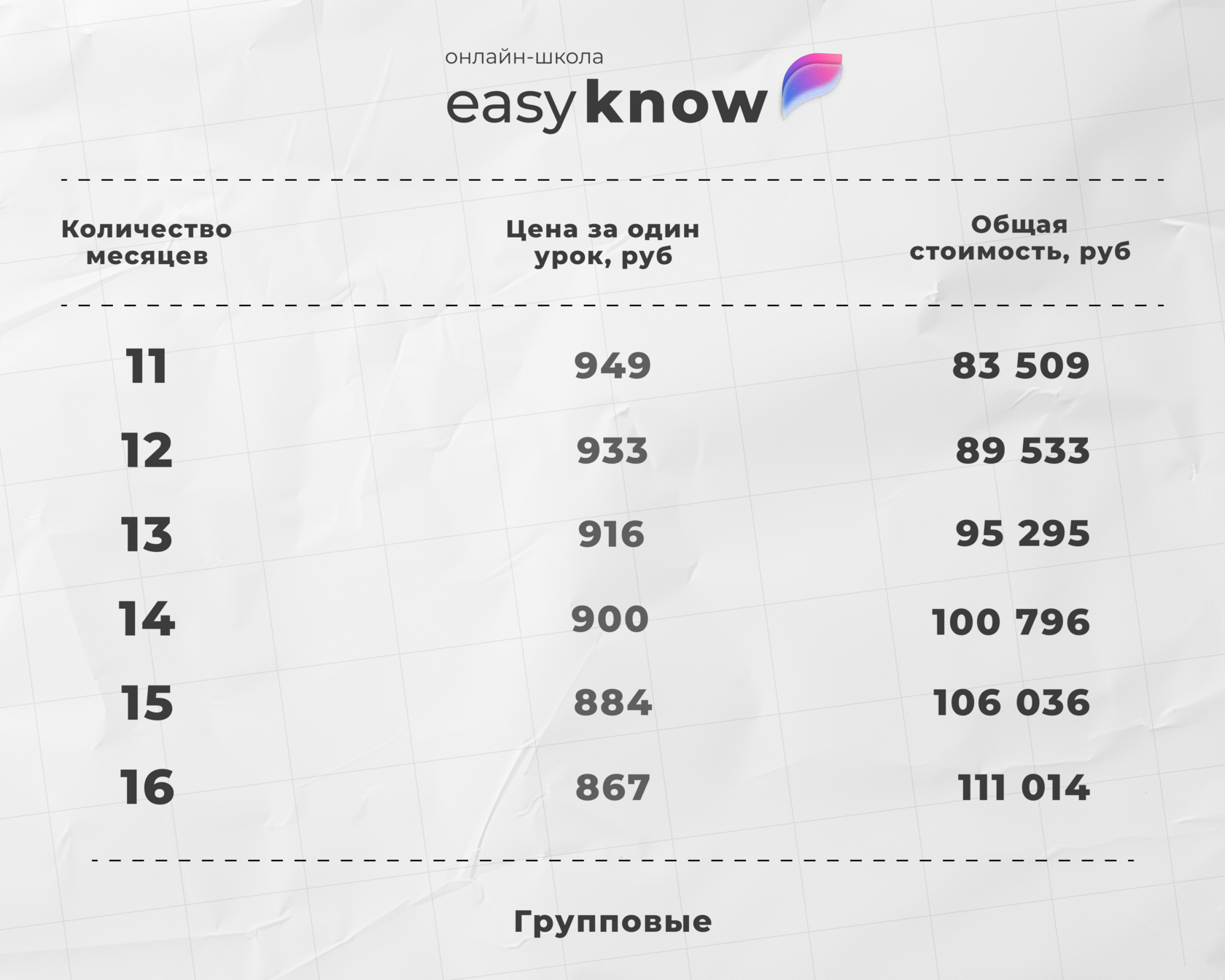
Переходите на платформу и получите скидку 40% на первый месяц занятий с репетитором. Скидка активируется сразу после регистрации.
Переходите на платформу и получите скидку 40% на первый месяц занятий с репетитором. Скидка активируется сразу после регистрации.